شیمی اسانس
ماهیت و منشاء اسانسهای گیاهی
اسانسها (Essential oils) تركيبات معطری هستند كه در اندامهای مختلف گياهان يافت میشوند و به علت تبخير در اثر مجاورت هوا آنها را روغنهای فرار مینامند (Volatile oils). اسانسها طبقهای از روغنهای گياهی هستند كه از مخلوط تركيبهای متنوع شيميايی فرار آلی تشكيل يافتهاند. در اصل وجود آنها مسئول بوی خوش در گياه میباشد. اسانسها در بسياری از گياهان عالی يافت میشوند. مهمترين تيرههايی كه داراي روغن فرار میباشند عبارتند از: تيره كاج، برگ بو، نارنج، مورد، چتريان، نعنائيان و كاسنی. اسانسها ممكن است به طور مستقيم توسط پروتوپلاسم به وسيله تجزيه مواد رزينی غشاء سلولها يا از هيدروليز بعضی از گليكوزيدها حاصل شوند. محل تشكيل و انباشت روغنهای فرار در گياهان در تيرههای مختلف گیاهی متفاوت است. به عنوان مثال در گياهان تيره نعنائيان روغنهای فرار در تارهای ترشح كننده، در تيره فلفل در سلولهای پارانشيم، در تيره چتريان در لولههای روغنی و در تيرههای كاج و نارنج در مجراهای ليزيژن و شيزوژن تشكيل میشوند.
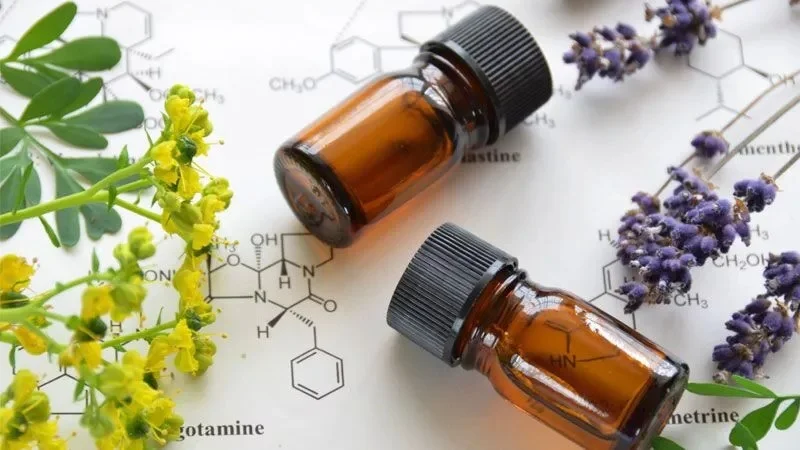
خواص فیزیکوشیمیایی اسانسها
اسانسها با اينكه از نظر تركيبهای شيميايی متفاوت هستند، ولی در بعضی از خواص فيزيكی مشترک میباشند. اسانسها بويی مشخص و ضريب شكست قوی دارند و در اكثر موارد روی نورپلاريزه مؤثر میباشند. میزان چرخش نور پلاریزه توسط اسانسها اغلب وسيلهای جهت تشخيص و تعیین کیفیت آنها میباشد. به طور مثال در اسانس نعناع تركيب منتول طبيعی چپگرد است، ولی نوع سنتزی آن راسميک میباشد. همچنين تركيب كامفور طبيعی چپگرد است، ولي كامفور سنتزی راسميک میباشد. وزن مخصوص اسانسها عموماً كمتر از آب است و فقط تعداد محدودی از اسانسهای گياهی چگالی بيشتر از آب دارند. به طور كلی اسانسها با آب غير قابل اختلاط میباشند، ولی میتوانند بوی خود را به آب انتقال دهند و ايجاد گلابهای (عرقیات) مختلف نمايند. اسانسها در الكل، اتر، پتروليوم اتر و اغلب حلالهای آلی محلول هستند. روغنهای فرار از نظر ويژگیهای شيميايی و فيزيكی با روغنهای دیگر تفاوت دارند كه مهمترين آنها عبارتند از:
- روغنهای فرار قابل تقطير شدن هستند و از اين جهت به راحتي میتوان آنها را از طريق روشهای تقطير استخراج نمود.
- ساختمان شيميايی روغنهای فرار برخلاف روغنهای ثابت از استرهای گليسيرين و اسيدهای چرب ساخته نشده است.
- روغنهای فرار برخلاف روغنهای ثابت لكههاي دائم روی كاغذ به جا نمیگذارند.
- روغنهای فرار برخلاف روغنهای ثابت با قلياها صابونی نمیگردند.
- روغنهای فرار فاسد نمیشوند بلكه در مجاورت هوا و نور، اكسيد شده و رزينی خواهند شد.

مواد شيميايی تشكيل دهنده اسانسها
اسانسها دارای مصارف ادويهای، دارويی و عطـرسازی هستند و اغلب از دو گـروه اصلی ترکیبات شیمیایی تشكيل شدهاند كه عبارتند از: ترپنها و فنيل پروپنها. از بين اين دو گروه، ترپنها فراوانتر و رايجتر هستند ولی در صورت حضور فنيل پروپنها، بايد آنها را عامل اصلی طعم و عطر دانست (نظير انيسون، رازيانه، ميخك هندی، دارچين و ريحان).
ترپنها
ترپنهای موجود در اسانسها را میتوان به دو گروه فرعی تقسيم نمود: مونوترپنها كه دارای ساختمان 10 كربنی بوده و سزكوييترپنها كه دارای ساختمان 15 كربنی میباشند. دیترپنها (20 كربنی) در اسانس بعضي گياهان (نظير زنجبيل) توليد میشوند و ولی در اغلب موارد کمیاب هستند. نكته مشترک موجود در ساختار كليه اين تركيبات، حضور بلوکهای 5 كربنی است كه به نام واحدهای ايزوپرن مشهورند. مونوترپنها از 2 واحد و سزكويیترپنها از 3 واحد ايزوپرنی تشكيل شدهاند. تقريباً ساختار اغلب مونوترپنهای غيرحلقوی بر يک ساختمان 10 كربنی بنا شده است و همچنين اساس ساختار مونوترپنهای يک حلقهای نيز يک هسته پارا- منتان میباشد.
تركيبات مونوترپنی دوحلقهای، از نظر ساختار كربنی تنوع زيادی دارند كه مهمترين آنها عبارتند از: كامفنها (camphene)، پيننها (pinene)، توجانها (thujane)، كارنها (carene) و فنچانها (fenchane). تغييرات بيشتر میتواند به يكی از روشهای افزوده شدن پيوند دوگانه (اكسيداسيون) يا حذف آن (احياء)، تركيب با اكسيژن به فرمهای الكلی (-OH)، كتونی (C=O)، آلدئيدی (-CHO) و استری (-OCO-) روی دهد. چند نمونه از ترکیباتی که در اثر اكسيداسيون و احياء ساختمان پارامنتان، در گياهان ایجاد شده اند، در شكل نشان داده شده است. البته تنوع در آرايش فضائی نیز میتواند منجر به ایجاد ساختارهای جدید شود. هر كربن با چهار گروه مختلف متصل به خود، يك مركز کایرال بالقوه بشمار میآيد. منتول 3 مرکز کایرال دارد و از نظر تئوری میتواند هشت (23) آرايش فضائی مختلف داشته باشد. از آنجايی كه سزكوئیترپنها، 5 كربن بيشتر از مونوترپنها دارند لذا تنوع ساختاری گستردهتری دارند. بطور كلی سزكوئیترپنها در مقايسه با مونوترپنها از فراريت کمتری نیز برخوردار میباشند.
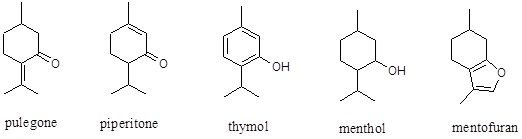
فنیل پروپنها
فنيل پروپنها، بدون استثناء در ساختار خود دارای يک حلقه 6 كربنی آروماتيك با يك زنجيره جانبی سه كربنه متصل به حلقه میباشند. زنجيره جانبی معمولاً حاوی يک پيوند دوگانه است ولی وجود اكسيژن در آن نادر است(نمونه اکسیژندار سينامالدئيد در اسانس دارچين). ممكن است تا چهار اتم اكسيژن روی حلقه آروماتيک جايگزين شده و سپس با تركيب يک گروه متيل، تغيير بيشتری يافته و توليد متيل اتر نمايد و يا نظير سافرول، يک حلقه اضافی متيل ايندوكسی تشكيل دهد.
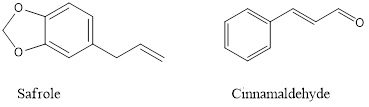
آزولنها
واژه آزولن براساس رنگ آبی اجزاء اسانس بابونه توسط پيس (Piesse) نامگذاری گرديد. آزولنها در اسانسهای زيادی از جمله اسانس كامفور، كبابه چينی، برنجاسف، گال بانوم، سنبل الطيب، و اسانس چند نمونه از اوكاليپتوسها ديده شدهاند. آزولنها در تركيبهای مختلف به رنگهاي آبی، بنفش و حتی سبز مشاهده میشوند. آزولنهای طبيعی در اسانسها به دو صورت یافت میشوند به این ترتیب که يا حضورشان رنگ قابل تشخيصی به اسانسها میدهند و يا به شكل مشتقات سزكوئیترپنها هستند كه با روشهای شيميايی يا فيزيكی قابل تبديل به آزولن رنگی میباشند. اين عمل میتواند توسط حرارت دادن و يا واكنش با اسيد، آبگيری و يا هيدروژنگيری به مورد اجراء درآيد. آزولنهای مختلف براساس رنگهايشان قابل تشخيص هستند و ممكن است با آبی خالص، آبی بنفش، بنفش، قرمز و حتی سبز مشخص شوند. براساس تحقيقات پلاتنر و پفاو تركيب مادر همه آزولنها هيدروكربور دو حلقهای C10H8 به نام عمومی آزولن میباشد.
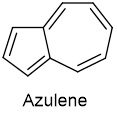
از نظر خواص شيميايی و فيزيكی آزولن تشابه زيادي به نفتالين دارد. اسكلت كربنی در آزولن نمايشگر اتصال يك حلقه پنج ضلعی با يك حلقه هفت ضلعی است كه اين ساختمان مسبب رنگ مشاهده شده توسط آزولنها است. آزولنها با سزكوئیترپنها مرتبط هستند. براساس فرضيه روزيكا اين هيدروكربنها در طبيعت از حلقوی شدن 3 مولكول زنجيرهای ايزوپرن بوجود میآيند. قويترين استدلال در مورد ارتباط بين سزكوئیترپنها و آزولنها بر اين پايه استوار است كه انواع سزكوئیترپنها و مشتقات آنها توسط هيدروژنگيری و يا آبگيری قابل تبديل به آزولن میباشند. ويژگی اصلی آزولنها طيف جذبی آنها است كه در طيف حوزه مرئی قرار میگيرد. اندازهگيری اين طيفها میتواند كمک مهمی در تعيين شماره اتمها و موقعيت استخلافها در سيستم حلقه آزولن محسوب گردد.
لطفاً نظر ارزشمند خود را درباره این مقاله در بخش دیدگاه بنویسید.


