اسید چیست؟
اسیدها ترکیبات شیمیایی هستند که ویژگیهای خاصی مانند طعم ترش، توانایی تغییر رنگ شناساگرها، و قابلیت واکنش با بازها برای تشکیل نمک و آب دارند. این مواد در صنایع مختلف، آزمایشگاهها، و حتی زندگی روزمره کاربرد دارند. در این مقاله به بررسی جامع خواص، انواع، کاربردها و خطرات اسیدها میپردازیم.
تعریف علمی اسید
در شیمی، اسید به مادهای گفته میشود که قادر به افزایش غلظت یونهای هیدروژن (⁺H) در محلول آبی است. این تعریف بر اساس نظریه آرنیوس ارائه شده است. نظریههای دیگری مانند برونستد-لوری و لوئیس نیز تعاریف متفاوتی از اسید ارائه میدهند:
نظریه برونستد-لوری: اسیدها دهندهی پروتون (⁺H) هستند.
نظریه لوئیس: اسیدها پذیرندهی جفتالکترون هستند.
خواص شیمیایی و فیزیکی اسیدها
طعمی ترش: اکثر اسیدها مزهای ترش دارند، مانند سیتریک اسید در لیمو.
رسانای الکتریسیته: محلولهای اسیدی به دلیل وجود یونها، رسانای الکتریکی هستند.
واکنش با فلزات: اسیدها با فلزات واکنش داده و گاز هیدروژن آزاد میکنند.
واکنش با بازها: اسیدها با بازها واکنش داده و نمک و آب تشکیل میدهند (واکنش خنثیسازی).
تغییر رنگ شناساگرها: اسیدها میتوانند رنگ شناساگرهایی مانند لیتموس را تغییر دهند.

طبقهبندی اسیدها
بر اساس منشأ
اسیدهای آلی: مانند استیک اسید که در سرکه یافت میشود.
اسیدهای معدنی: مانند سولفوریک اسید که در صنعت کاربرد فراوان دارد.

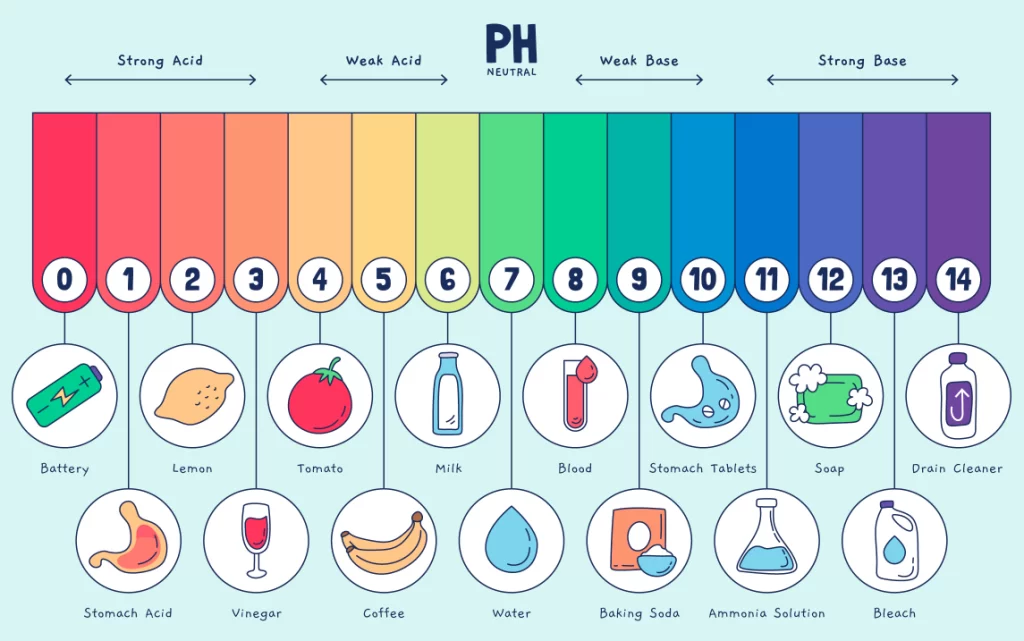
بر اساس قدرت
اسیدهای قوی: مانند کلریدریک اسید که به طور کامل یونیزه میشوند.
اسیدهای ضعیف: مانند استیک اسید که به صورت جزئی یونیزه میشوند.
بر اساس حالت فیزیکی
مایع: مانند سولفوریک اسید
جامد: مانند سیتریک اسید
گاز: مانند هیدروکلریک اسید در فاز گازی
کاربردهای اسیدها
در صنعت
تولید کودهای شیمیایی: نیتریک اسید و فسفریک اسید در تولید کودها استفاده میشوند.
ساخت پلاستیک: اسیدها در فرآیندهای تولید مواد پلیمری نقش دارند.
صنایع غذایی: اسیدها به عنوان تنظیمکننده pH و نگهدارنده به کار میروند.
در پزشکی و داروسازی
ساخت دارو: بسیاری از داروها حاوی ترکیبات اسیدی هستند.
تحقیقات آزمایشگاهی: برای انجام آزمایشهای بیوشیمیایی.
در زندگی روزمره
نظافت: اسیدهایی مانند استیک اسید در پاککنندههای خانگی به کار میروند.
خوراکیها: سیتریک اسید به عنوان ماده افزودنی در غذاها استفاده میشود.
خطرات و نکات ایمنی
۱. سوختگی شیمیایی
اسیدها میتوانند باعث سوختگی شدید پوست و چشم شوند. در صورت تماس با اسید، باید فوراً محل تماس را با آب فراوان شستوشو داد.
۲. استنشاق بخارات
بخارات برخی اسیدها مانند هیدروکلریک اسید میتوانند به سیستم تنفسی آسیب برسانند. استفاده از تهویه مناسب و ماسک ضروری است.
۳. ذخیرهسازی ایمن
اسیدها باید در ظروف مقاوم به خوردگی و در مکانهای خنک و دور از مواد قابل اشتعال نگهداری شوند.
نمونههایی از اسیدهای رایج
۱. سولفوریک اسید (H₂SO₄)
کاربرد: تولید باتری، تصفیه نفت.
خطر: بسیار خورنده و واکنشپذیر.
۲. کلریدریک اسید (HCl)
کاربرد: تمیز کردن فلزات، تولید پلاستیک.
خطر: بخارات آن باعث تحریک سیستم تنفسی میشود.
۳. نیتریک اسید (HNO₃)
کاربرد: تولید کودهای شیمیایی و مواد منفجره.
خطر: بسیار سمی و خورنده.
۴. استیک اسید (CH₃COOH)
کاربرد: افزودنی غذایی، تولید پلاستیک.
خطر: در غلظتهای بالا محرک است.
اسیدها دستهای از مواد شیمیایی پرکاربرد هستند که در صنایع مختلف، پزشکی و حتی زندگی روزمره نقشی حیاتی ایفا میکنند. با این حال، به دلیل خاصیت خورندگی و واکنشپذیری بالا، رعایت نکات ایمنی در استفاده و نگهداری آنها ضروری است.
لطفاً نظر ارزشمند خود را درباره این مقاله بنویسید.

