خواص منحصر به فرد آب
آب یک ماده رایج روی زمین است که اغلب ما خواص منحصر به فرد آن را نادیده میگیریم. تمام فرآیندهای حیات شامل آب است. با اینکه آب هیچ نوع کالری یا مواد مغذی آلی ندارد، وجودش برای ادامه حیات، الزامی است و در صورت اتمام آن، حیات روی کره زمین پایان خواهد یافت. آب یک حلال عالی برای بسیاری از ترکیبات یونی و همچنین برای سایر موادی است که قادر به تشکیل پیوند هیدروژنی با آب هستند.
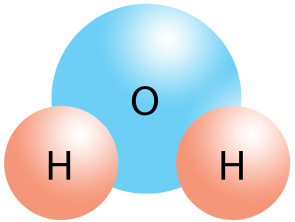
ساختار آب
آب از دو اتم هیدروژن و یک اتم اکسیژن تشکیل شده است. هر یک از دو اتم هیدروژن با اتم اکسیژن پیوند کووالانسی دارند و یک شکل چهار وجهی را تشکیل میدهند. مولکول آب به دلیل اثر دافعه جفت الکترونهای تنها روی اکسیژن خمیده میشود. زاویه پیوند (H-O-H) 104.5 درجه است.
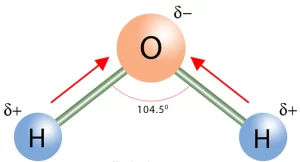
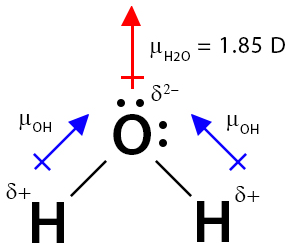
قطبیت و ممان دوقطبی مولکول آب
آب به دلیل شکل نامتقارنش یک مولکول قطبی است. اتم اکسیژن الکترونگاتیوتر از اتم هیدروژن است و الکترونهای پیوندی را به سمت خود جذب میکند و بار جزئی منفی به خود میگیرد. از سوی دیگر، دو اتم هیدروژن بار جزئی مثبت دارند. بنابراین، پیوند O-H قطبی است. آب شکل خمیدهای (زاویهدار) دارد که باعث ایجاد یک گشتاور دوقطبیِ خالصِ برابر با 1.855 D میشود. مولکولهای آب به دلیل قطبیت، پیوند هیدروژنی تشکیل میدهند.
حلال جهانی
آب به عنوان حلال جهانی نامیده میشود. بسیاری از گونههای قطبی و یونی را در خود حل میکند. این ویژگی برای موجودات زنده مفید است، چون آب مواد مغذی ضروری را به بخشهای عملکردی مختلف با خود حمل میکند. اگرچه آب بسیاری از مواد را حل میکند، اما روغنها، چربیها و برخی هیدروکسیدها در آب حل نمیشوند.
ظرفیت حرارتی بالا
آب ظرفیت گرمایی بالایی دارد، به این معنی که برای گرم کردن آب باید انرژی زیادی مصرف شود. به طور دقیق، آب به ازای هر کیلوگرم، 4184 ژول گرما جذب میکند تا دمای آن 1 درجه سانتیگراد افزایش یابد. این ویژگی به تعدیل دمای زمین کمک میکند، چون آب گرما را در طول روز در خود به دام میاندازد و به تدریج در طول شب این گرما را آزاد می کند، در نتیجه دمای زمین زیاد تغییر نمیکند.
گرمای تبخیر بالا
آب گرمای تبخیر بالایی دارد. این ویژگی به ما کمک میکند در یک روز گرم تابستانی خنک شویم. برای تبخیر کاملِ هر گرم آب و تبدیل آن به بخار، 2260 ژول انرژی نیاز است. عرق از آبی تشکیل شده است که از پوست ما تبخیر میشود. گرمای بیش از حد را از بدن ما منتقل کرده و ما را خنک و راحت میکند. این فرآیند به عنوان خنک کننده تبخیری شناخته میشود.
خاصیت کشش سطحی آب
مولکولهای آب در کنار هم قرار گرفته و با یکدیگر پیوندهای هیدروژنی قوی ایجاد میکنند و در نتیجه نیروهای جاذبه قوی بین آنها وجود دارد. هر مولکول از همه جهات کشیده میشود. در سطح آب، مولکولها فقط از طرفین و پایین کشیده میشوند، نه از بالا. آب، لایهای (مانند پوست) را روی سطح تشکیل میدهد که میتواند در برابر نیروی خارجی مقاومت کند. این خاصیت آب به کشش سطحی معروف است. مقدار کشش سطحی آب برابر با Jm2 0.072 است.

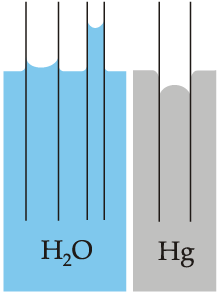
خاصیت چسبندگی و اثر مویینگی
مولکولهای آب میتوانند به سطوح نیز بچسبند. این خاصیت به چسبندگی معروف است. مولکولهای آب که به دیوارههای ظرف میچسبند، نیرویی به سمت بالا در لبهها ایجاد میکنند و منجر به شکل تقعری میشود (شکل زیر ر ببینید). از سوی دیگر، خاصیت چسبندگی باعث میشود مولکولهای آب در کنار هم بمانند. اثر مویینگی باعث حرکت مولکولهای آب میشود. این حالت زمانی اتفاق میافتد که چسبندگی به دیوارهها قویتر از چسبندگی بین مولکولهای مایع باشد. این پدیده برای گیاهان و درختان ضروری است و به این ترتیب آب و تمام مواد مغذی محلول میتوانند در برابر گرانش به سمت بالا حرکت کنند.
چگالی
آب هنگام یخ زدن متراکم میشود. چگالی یخ کمتر از آب است و به همین دلیل یخ روی آب شناور میشود. این پدیده را میتوان در دریاچهها در روزهای یخبندان مشاهده کرد که لایه ضخیمی از یخ سطح دریاچه را میشاند. یخ گرما را داخل دریاچه حفظ میکند و از یخ زدن آن جلوگیری میکند. به این ترتیب ماهیها و سایر موجودات زنده میتوانند در زیر آب زنده بمانند.

حالت جامد (یخ)
وقتی آب منجمد میشود، یخ تشکیل میشود. یخ ماده متراکمی است که در آن مولکولها به یکدیگر نزدیک هستند و بین آنها پیوند هیدروژنی وجود دارد و در نتیجه ساختار بلوری شش ضلعی ایجاد میشود. یخِ خالص شفاف است. اگر ذرات خاک و حبابهای هوا وجود داشته باشد، ممکن است به رنگِ آبیِ مات به نظر برسد. یخ برای خنک کردن، ورزش های زمستانی و مجسمه سازی روی یخ استفاده میشود.
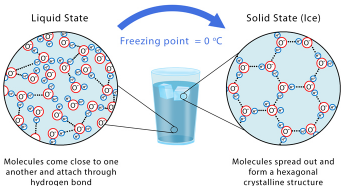
حالت مایع
آب در دمای اتاق در حالت مایع است. مایع بودن ترکیبی که در ساختارش کربن ندارد در دمای اتاق امری بسیار غیر عادی است. مولکولهای آب پیوندهای هیدروژنی کمتری نسبت به یخ تشکیل میدهند که به آنها اجازه میدهد به سرعت حرکت کنند.
حالت گازی (بخار آب)
آب در حالت گازی، بخار داغ تشکیل میدهد. با شکستن پیوندهای هیدروژنی، مولکولها از هم جدا میشوند. عدم وجود پیوندهای هیدروژنی باعث میشود که بخار در تماس با پوست بسیار خطرناک باشد. مولکولهای بخار انرژی حاصل از شکستن پیوند هیدروژنی را حمل میکنند. هنگامی که آنها به پوست صورت برخورد میکنند، بخار از طریق یک فرآیند گرمازا به آبِ مایع تبدیل میشود و گرمای آزاد شده از این فرایند منجر به سوختگی پوست میشود.
نقاط انجماد و جوش
آب در دمای صفر درجه سانتیگراد یخ میزند و در دمای 100 درجه سانتیگراد میجوشد. نقطه جوش بالا به این دلیل است که آب برای شکستن پیوندهای هیدروژنیِ قبل از جوشش، به انرژی زیادی نیاز دارد. به همین ترتیب، انرژی عظیمی برای ذوب شدن یخ مورد نیاز است. از آنجایی که یخ و آب برای تبدیل فاز به انرژی بسیار زیادی نیاز دارند، ذوب و تبخیر کند است. این ویژگی برای اکوسیستم، به ویژه موجودات زنده، حیاتی است تا در زیر آب زنده بمانند.
جمعبندی
خواص منحصر به فرد آب در شکل زیر خلاصه شده است.
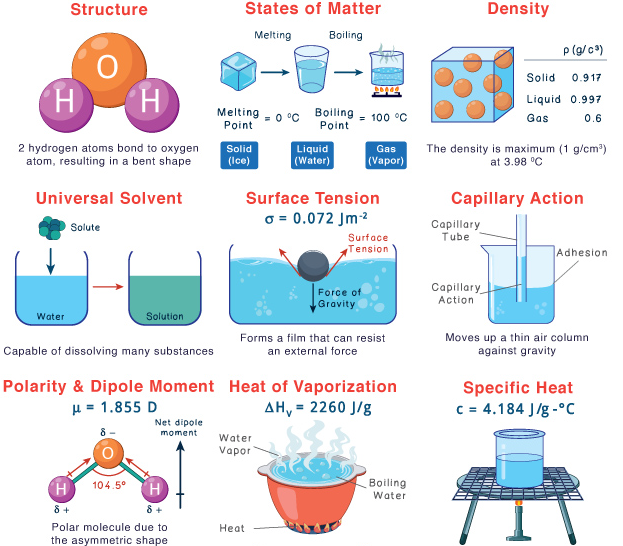
لطفاً نظر ارزشمند خود را درباره این مقاله بنویسید.


