قانون اول ترمودینامیک چیست؟
قوانین ترمودینامیک مجموعهای از قوانین هستند که یک سیستم فیزیکی را در تعادل حرارتی توصیف میکنند. این قوانین چندین کمیت ترمودینامیکی مهم مانند انرژی داخلی، گرما، دما، آنتالپی و آنتروپی را تعریف کرده و بین این پارامترها ارتباط برقرار میکنند. قوانین ترمودینامیک، قوانین اساسی فیزیک هستند و در سایر شاخههای علوم طبیعی نیز استفاده میشوند.
قانون اول ترمودینامیک از اصل بقای انرژی استفاده میکند. این قانون رابطهای بین انرژی داخلی یک سیستم، انتقال حرارت و کار انجام شده برقرار میکند. طبق قانون اول، تغییر در انرژی داخلی برابر با گرمای داده شده به سیستم منهای کار انجام شده توسط سیستم است.
اصل بقای انرژی بیان میکند که انرژی نه میتواند خود به خود ایجاد شود و نه از بین برود. فقط از یک شکل به شکل دیگر تبدیل میشود.
فیزیکدان آلمانی رودولف کلازیوس اولین کسی بود که قانون اول ترمودینامیک را در سال 1850 ارائه کرد.
معادله قانون اول ترمودینامیک
یک سیستم و محیط اطراف آن را در نظر بگیرید. از نظر ریاضی، قانون اول ترمودینامیک با رابطه زیر بیان میشود.
ΔU = Q – W
در این معادله:
ΔU: تغییر در انرژی داخلی سیستم
Q: گرمای اضافه شده به سیستم
W: کار انجام شده توسط سیستم
واحد: ژول یا J
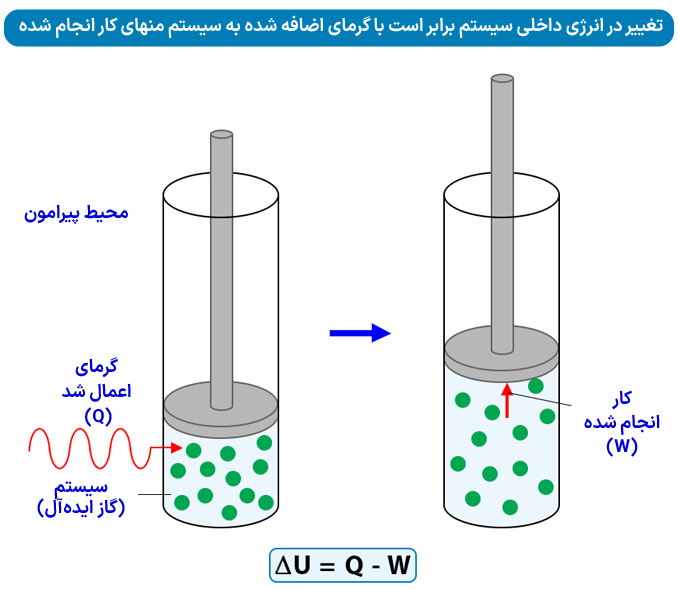
قانون اول ترمودیامیک فرض میکند که هیچ مادهای بین سیستم و محیط اطراف منتقل نمیشود و فقط انرژی به صورت گرما مبادله میشود. این نوع سیستم به سیستم بسته معروف است.
زمانیکه که روی سیستم کار انجام شود، معادله اولین قانون ترمودینامیک به شکل زیر تغییر میکند:
ΔU = Q + W
از آنجایی این دو رابطه، معادل هم هستند:
کار انجام شده توسط سیستم = – کار انجام شده روی سیستم
وقتی کار روی سیستم انجام میشود، انرژی داخلی را افزایش میدهد. بنابراین، در این معادله ΔU = Q + W علامت مثبت میشود. هنگامی که سیستم کار میکند، انرژی داخلی آن کاهش مییابد. بنابراین، در این معادله ΔU = Q – W علامت منفی میشود.
برای یک سیستم ایزوله، که در آن تبادل گرما و ماده بین سیستم و محیط اطراف وجود ندارد، Q = 0 و ΔU = – W.
مثالهایی از قانون اول ترمودینامیک در زندگی روزمره
- ذوب مکعبهای یخ نمونهای معمولی از قانون اول ترمودینامیک است. یخ گرما را از محیط اطراف جذب میکند و هوا را خنک میکند. تبادل گرما ادامه مییابد تا یخها ذوب شوند.
- خوردن، مثال دیگری از قانون اول ترمودینامیک است. متابولیسم انسان شامل تبدیل غذا به گرما، کار و چربی ذخیره شده است.
- روشن کردن کتری برقی نمونه دیگری از قانون اول است. وقتی کلید را روشن میکنیم، برق، کتری را روشن میکند که آب را گرم میکند.
قانون اول ترمودینامیک و موتورهای حرارتی
رایجترین کاربرد قانون اول ترمودینامیک موتورهای حرارتی هستند. موتورهای حرارتی انرژی حرارتی را به انرژی مکانیکی و بالعکس تبدیل میکنند. اصل اساسی موتورهای حرارتی این است که بین گرما، حجم و فشار یک سیال در حال کار مانند گاز، رابطه برقرار میکنند.
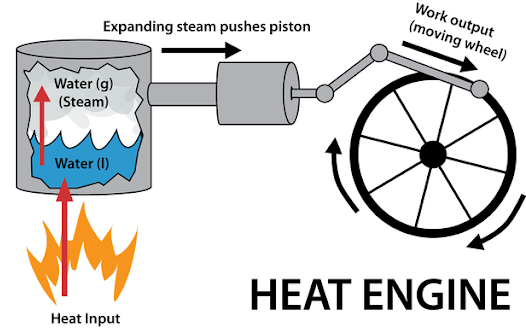
وقتی گاز گرم میشود، منبسط میگردد. اما اگر از انبساط آن جلوگیری شود، به دیوارههای ظرف فشار وارد میکند. فرض کنید گاز در داخل یک سیلندر با یک پیستون متحرک محبوس شده است. در این حالت، گاز به سطح پیستون نیرو وارد میکند و به آن اجازه حرکت میدهد. حرکت پیستون را میتوان برای انجام کاری مهار کرد که مقدار آن از حاصل ضرب نیرو و فاصله حرکت پیستون بدست میآید.
قانون اول چنین ایجاب میکند که موتورهای حرارتی نتوانند بیش از گرمای تولید شده کار تولید کنند. این محدودیت نشان میدهد که راندمان حرارتی موتور که به عنوان نسبت کار انجام شده به گرمای عرضه شده تعریف میشود، نمیتواند بیشتر از 100٪ باشد.
جمعبندی
چهار قانون ترمودینامیک وجود دارد: قانون صفرم، قانون اول، قانون دوم و قانون سوم.
بیان قانون اول ترمودینامیک: هنگامی که انرژی به یک سیستم اعمال میشود یا از آن خارج میشود، انرژی داخلی سیستم مطابق با اصل بقای انرژی تغییر میکند.
به عبارت دیگر، انرژی هرگز نمیتواند خود به خود ایجاد شود یا از بین برود، بلکه از شکلی به شکل دیگر تبدیل میشود. افزایش انرژی سیستم معادل از دست دادن انرژی توسط محیط پیرامون است. به طور مشابه، از دست دادن انرژی توسط سیستم معادل افزایش انرژیِ محیط اطراف است.
لطفاً نظر ارزشمند خود را درباره این مقاله بنویسید.



